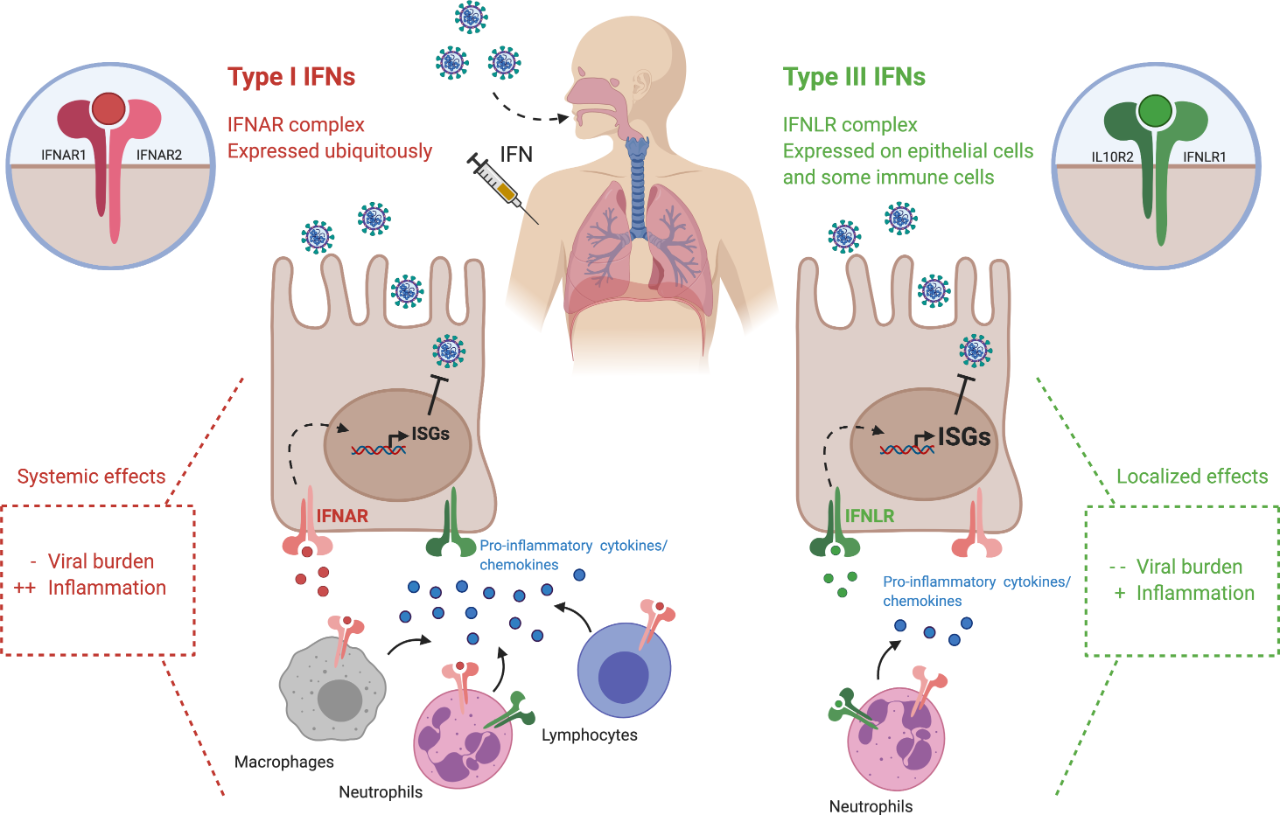
Interferon is een signaal dat door het virus wordt afgescheiden aan de nakomelingen van het lichaam om het immuunsysteem te activeren en vormt een verdedigingslinie tegen het virus. Type I-interferonen (zoals alfa en bèta) worden al tientallen jaren bestudeerd als antivirale middelen. Type I-interferonreceptoren komen echter in veel weefsels tot expressie, waardoor toediening van type I-interferon gemakkelijk kan leiden tot een overreactie van de immuunrespons van het lichaam, met een reeks bijwerkingen tot gevolg. Het verschil is dat type III-interferonreceptoren (λ) alleen tot expressie komen in epitheelweefsel en bepaalde immuuncellen, zoals de longen, luchtwegen, darmen en lever, waar het nieuwe coronavirus werkzaam is, waardoor interferon λ minder bijwerkingen heeft. PEG-λ wordt gemodificeerd door polyethyleenglycol op basis van natuurlijk interferon λ en de circulatietijd in het bloed is aanzienlijk langer dan die van natuurlijk interferon. Verschillende studies hebben aangetoond dat PEG-λ een breedspectrum antivirale activiteit heeft.
Al in april 2020 publiceerden wetenschappers van het National Cancer Institute (NCI) in de Verenigde Staten, King's College London in het Verenigd Koninkrijk en andere onderzoeksinstellingen commentaren in J Exp Med waarin ze klinische studies aanbeveelden met interferon λ voor de behandeling van Covid-19. Raymond T. Chung, directeur van het Hepatobiliary Center van het Massachusetts General Hospital in de Verenigde Staten, kondigde in mei ook aan dat er een door onderzoekers geïnitieerd klinisch onderzoek zou worden uitgevoerd om de werkzaamheid van PEG-λ tegen Covid-19 te evalueren.
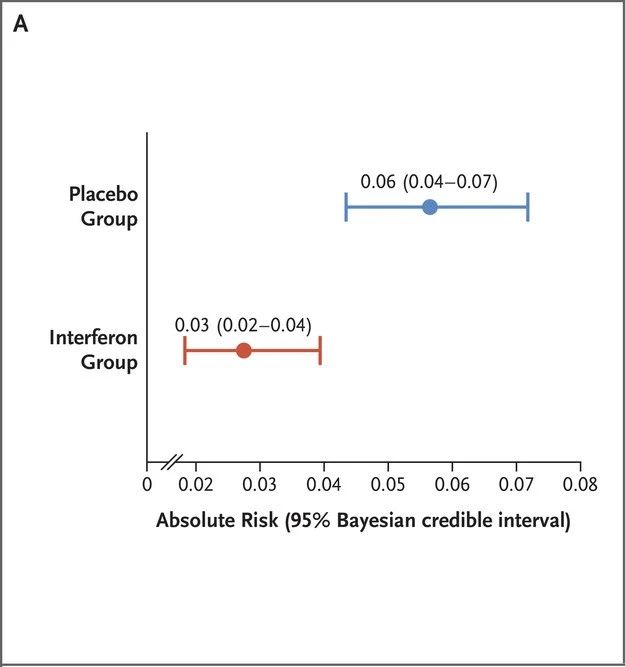
Uit twee klinische fase 2-onderzoeken is gebleken dat PEG-λ de virale lading bij COVID-19-patiënten aanzienlijk kan verminderen [5,6]. Op 9 februari 2023 publiceerde het New England Journal of Medicine (NEJM) de resultaten van een adaptief fase 3-onderzoek genaamd TOGETHER, onder leiding van Braziliaanse en Canadese wetenschappers, waarin het therapeutische effect van PEG-λ op COVID-19-patiënten verder werd geëvalueerd [7].
Poliklinische patiënten met acute COVID-19-symptomen en binnen 7 dagen na aanvang van de symptomen kregen PEG-λ (eenmalige subcutane injectie van 180 μg) of placebo (eenmalige injectie of oraal). De primaire samengestelde uitkomstmaat was ziekenhuisopname (of verwijzing naar een tertiair ziekenhuis) of bezoek aan de spoedeisende hulp vanwege COVID-19 binnen 28 dagen na randomisatie (observatie > 6 uur).
Het nieuwe coronavirus muteert sinds de uitbraak. Daarom is het bijzonder belangrijk om te onderzoeken of PEG-λ een genezende werking heeft op verschillende varianten van het nieuwe coronavirus. Het team voerde subgroepanalyses uit van de verschillende stammen van het virus die patiënten in deze studie infecteerden, waaronder Omicron, Delta, Alpha en Gamma. De resultaten toonden aan dat PEG-λ effectief was bij alle patiënten die met deze varianten waren geïnfecteerd, en het meest effectief bij patiënten die met Omicron waren geïnfecteerd.
Qua viral load had PEG-λ een significanter therapeutisch effect bij patiënten met een hoge viral load, terwijl er geen significant therapeutisch effect werd waargenomen bij patiënten met een lage viral load. Deze werkzaamheid is vrijwel gelijk aan die van Paxlovid (Nematovir/Ritonavir) van Pfizer.
Opgemerkt moet worden dat Paxlovid oraal wordt toegediend in de vorm van 3 tabletten, tweemaal daags, gedurende 5 dagen. PEG-λ daarentegen vereist slechts één subcutane injectie om dezelfde werkzaamheid te bereiken als Paxlovid, waardoor de therapietrouw beter is. Naast therapietrouw heeft PEG-λ nog andere voordelen ten opzichte van Paxlovid. Studies hebben aangetoond dat Paxlovid gemakkelijk geneesmiddelinteracties kan veroorzaken en het metabolisme van andere geneesmiddelen kan beïnvloeden. Mensen met een hoge incidentie van ernstige COVID-19, zoals oudere patiënten en patiënten met chronische aandoeningen, gebruiken medicijnen vaak langdurig, waardoor het risico op Paxlovid in deze groepen aanzienlijk hoger is dan bij PEG-λ.
Paxlovid is bovendien een remmer die zich richt op virale proteasen. Als het virale protease muteert, is het medicijn mogelijk niet effectief. PEG-λ bevordert de eliminatie van virussen door de lichaamseigen immuniteit te activeren en richt zich niet op een virusstructuur. Daarom wordt verwacht dat PEG-λ zijn werkzaamheid behoudt, zelfs als het virus in de toekomst verder muteert.
De FDA gaf echter aan dat ze het noodgebruik van PEG-λ niet zou goedkeuren, tot grote teleurstelling van de wetenschappers die bij het onderzoek betrokken waren. Eiger zegt dat dit mogelijk komt doordat het onderzoek niet in een Amerikaans klinisch onderzoekscentrum plaatsvond en doordat het onderzoek werd geïnitieerd en uitgevoerd door de onderzoekers, niet door de farmaceutische bedrijven. Als gevolg hiervan zal PEG-λ aanzienlijk veel geld en meer tijd moeten investeren voordat het in de Verenigde Staten kan worden gelanceerd.
Als breedspectrum antiviraal middel richt PEG-λ zich niet alleen op het nieuwe coronavirus, maar kan het ook de klaring van andere virale infecties door het lichaam verbeteren. PEG-λ heeft mogelijke effecten op het influenzavirus, het respiratoir syncytieel virus en andere coronavirussen. Sommige studies suggereren ook dat λ-interferonen, mits vroegtijdig toegepast, kunnen voorkomen dat het virus het lichaam infecteert. Eleanor Fish, immunoloog aan de Universiteit van Toronto in Canada en niet betrokken bij de TOGETHER-studie, zei: "Dit type interferon zou het meest preventief gebruikt worden, met name om personen met een hoog risico te beschermen tegen infectie tijdens uitbraken."
Plaatsingstijd: 29-07-2023