Gemengde hyperlipidemie wordt gekenmerkt door verhoogde plasmaspiegels van low-density lipoproteïnen (LDL) en triglyceriderijke lipoproteïnen, wat leidt tot een verhoogd risico op atherosclerotische cardiovasculaire aandoeningen bij deze patiëntenpopulatie.
ANGPTL3 remt lipoproteïnelipase en endosepiase, evenals de opname van triglyceriderijke lipoproteïnen in de lever. Dragers van de geïnactiveerde ANGPTL3-variant hadden lagere niveaus van triglyceriden, LDL-cholesterol, high-density lipoproteïne (HDL)-cholesterol en non-HDL-cholesterol, evenals een lager risico op atherosclerotische cardiovasculaire aandoeningen. Zodasiran is een small interfering RNA (RNAi)-medicijn dat de ANGPTL3-expressie in de lever aanpakt.
Gemengde hyperlipidemie verwijst naar verhoogde waarden van low-density lipoproteïne cholesterol (LDL-C) en triglyceriderijke lipoproteïnen. Triglyceriderijke lipoproteïnen (waaronder chylomicronen, very low density lipoproteïnen (VLDL) en restcholesterol) spelen een belangrijke rol bij het ontstaan van atherosclerotische aandoeningen. Er is geen effectieve behandeling voor gemengde hyperlipidemie.
Het is bekend dat Bates de triglyceridenspiegel (TG) verlaagt, maar de verlaging is beperkt. Tegelijkertijd hebben TG-verlagende medicijnen, waaronder Bates (zoals eicosapentaeenzuur, enz.), geen significant effect op het risico op atherosclerotische aandoeningen veroorzaakt door een verhoogd restcholesterolgehalte. Bovendien hebben eerdere studies bij patiënten die al statines gebruiken aangetoond dat gecombineerde TG-verlagende medicijnen het risico op cardiovasculaire aandoeningen niet verminderen. Deze factoren maken de behandeling van gemengde hyperlipidemie zeer moeilijk.
ANGPTL3 (angiopoietine-achtig proteïne 3) reguleert het metabolisme van lipiden en lipoproteïnen, waaronder TG en non-high-density lipoproteïne cholesterol (HDL-C), door de opname van lipoproteïnelipase, endosepiase en LDL-receptorafhankelijke hepatische lipoproteïnen (LDL-receptoren) reversibel te remmen. Gebleken is dat de inactivatievariant van ANGPTL3 leidt tot verhoogde activiteit van lipoproteïnelipase en endosepiase, wat in de meeste gevallen leidt tot lage plasmalipoproteïnespiegels. Deze omvatten triglyceriderijke lipoproteïnen (d.w.z. chylomicronen, restcholesterol, VLDL, medium-density lipoproteïne [IDL]), LDL, high-density lipoproteïne (HDL), lipoproteïne (a) en hun cholesterolcomponenten. Heterozygote mensen die drager zijn van deze variant hebben een ongeveer 40% lager risico op atherosclerotische ziekte en er zijn geen nadelige klinische fenotypen gevonden. ANGPTL3 komt tot expressie in de lever en gen-silencing therapieën die zich richten op het mRNA ervan, zogenaamde small interfering RNA (siRNA) drugs, vormen een veelbelovende hybride behandeling voor hyperlipidemie.
Op 12 september 2024 publiceerde het New England Journal of Medicine (NEJM) een ARCHES 2-studie die bevestigde dat het siRNA-medicijn zodasiran de TG-waarden significant verlaagde bij patiënten met gemengde hyperlipidemie [1]. ARCHES-2 is een dubbelblinde, placebogecontroleerde, fase 2b-studie met een exploratie van het dosisbereik. In totaal namen 204 patiënten met gemengde hyperlipidemie (nuchtere TG-waarden 150-499 mg/dl, LDL-C-waarden ³70 mg/dl of niet-HDL-C-waarden ³100 mg/dl) deel aan de studie. Ze werden verdeeld in een zodasiran-groep van 50 mg, een 100 mg-groep, een 200 mg-groep en een placebocontrolegroep. Patiënten kregen subcutane injecties in week 1 en 12 en kregen follow-upprofylaxe tot week 36.
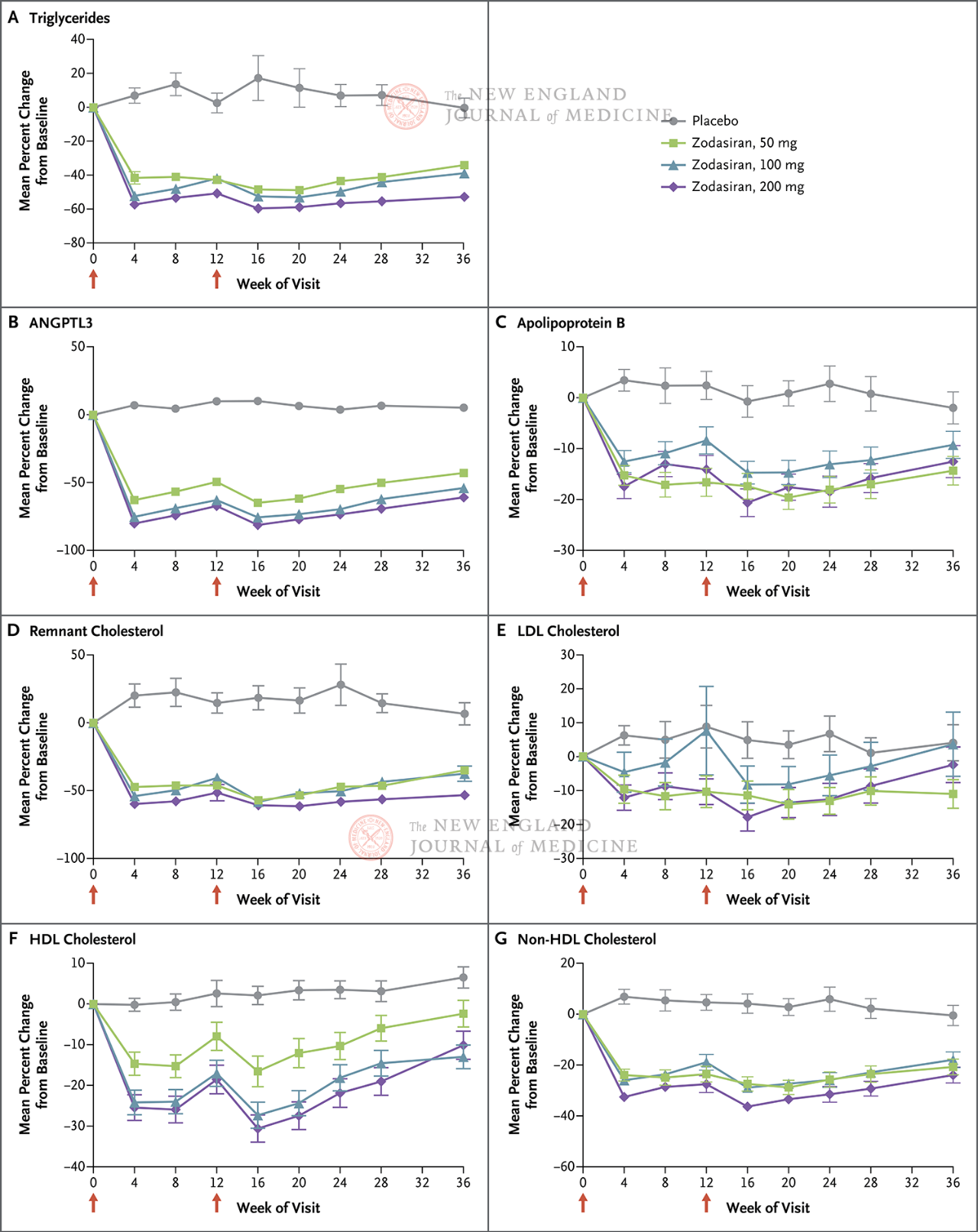
Het primaire eindpunt was de procentuele verandering in TG van baseline tot week 24. Uit de studie bleek dat de TG-waarden in de zodasirangroep in week 24 significant waren verlaagd op een dosisafhankelijke manier (de TG-waarden in elke dosisgroep waren verlaagd met respectievelijk 51, 57 en 63 procentpunten, vergeleken met die in de placebogroep) (P < 0,001 voor alle vergelijkingen). ANGPTL3 daalde ook met respectievelijk 54 procentpunten, 70 procentpunten en 74 procentpunten. De niet-HDL-C-waarden daalden met 29 procentpunten, 29 procentpunten en 36 procentpunten, de apolipoproteïne B-waarden daalden met 19 procentpunten, 15 procentpunten en 22 procentpunten, en de LDL-C-waarden daalden met respectievelijk 16 procentpunten, 14 procentpunten en 20 procentpunten, en deze resultaten hielden aan tot de 36e week. In week 24, zodasiran
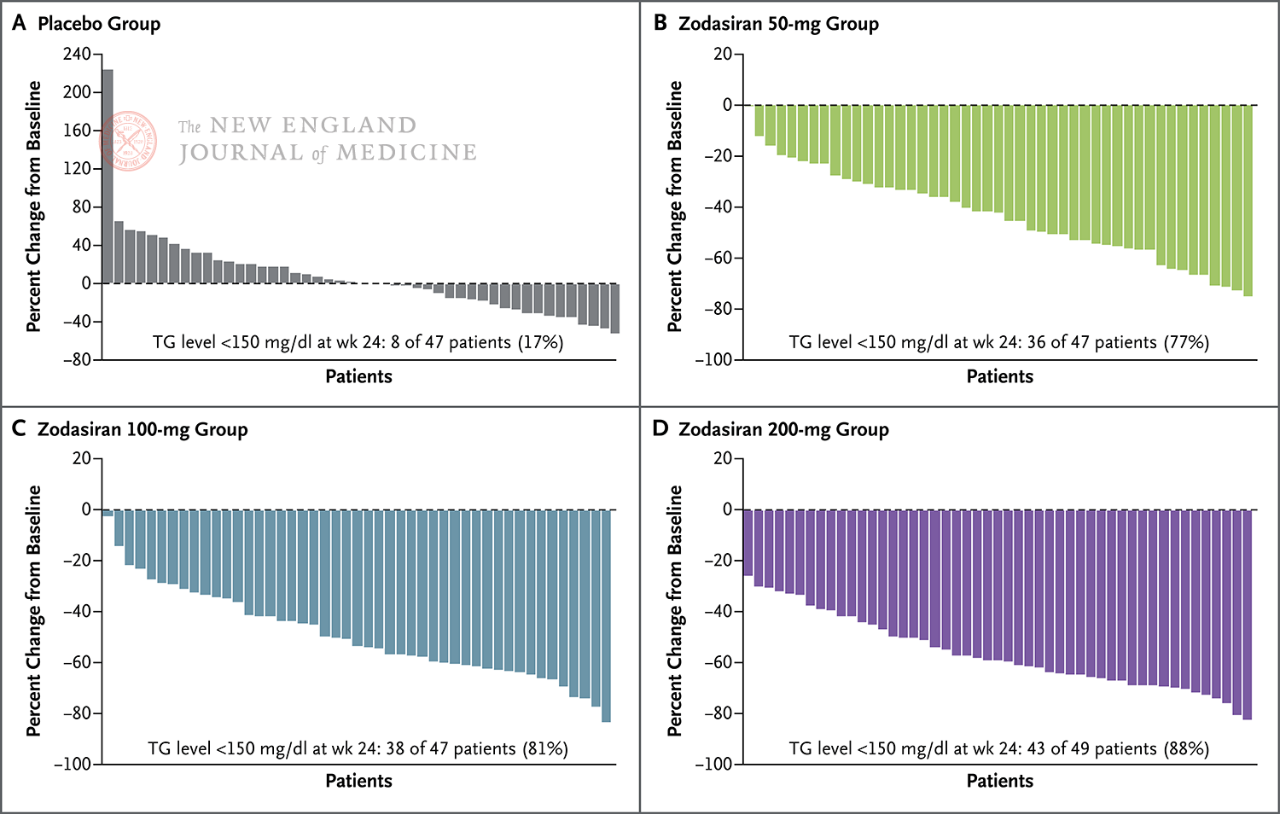
Bij 88% van de patiënten in de 200 mg-groep was de nuchtere TG gedaald tot het normale bereik.
Rode pijlen op dag 1 en 12 geven toediening van zodasiran of placebo aan.
De nuchtere TG-waarden daalden in week 24 naar normaal (150
mg/dL of minder)
Elke pijler vertegenwoordigt één patiënt.
Uit de studie bleek ook dat zotasiran veilig was in alle doseringsgroepen. Slechts twee patiënten (één in de placebogroep en één in de 100 mg zotasirangroep) stopten met de studie vanwege bijwerkingen. Alle ernstige bijwerkingen in de zotasirangroep herstelden aan het einde van de studie en er was één sterfgeval in de placebogroep. De enige zorgwekkende bijwerking was een stijging van HBA1c in de 200 mg zotasirangroep vergeleken met placebo (gemiddelde verandering van baseline tot week 24 [±SD], 0,38±0,66% versus -0,03±0,88% bij patiënten met reeds bestaande diabetes). Patiënten zonder diabetes hadden een stijging van 0,12±0,19% versus -0,03±0,19%.
Bijna alle patiënten in de studie (96%) werden behandeld met statines (waarvan 37% hooggedoseerde statines), 1% werd behandeld met een proproteïneconverterend enzym subtilysine 9-remmer (PCSK9i) en 21% werd behandeld met fibraten. De toevoeging van zodasiran aan het huidige conventionele behandelregime leidde daarom nog steeds tot aanzienlijke lipidenverlagende effecten, wat in de toekomst een nieuw regime biedt voor de behandeling van gemengde hyperlipidemie.
In week 24 verlaagde de maximale dosis van 200 mg zotasiran in de studie het restcholesterolgehalte met 34,4 mg/dl vergeleken met placebo. Op basis van de huidige modellen wordt verwacht dat deze verlaging ernstige cardiale bijwerkingen met 20 procent zal verminderen. Zodasiran kan potentieel worden gebruikt als monotherapie voor alle lipoproteïnecomponenten om het risico op cardiovasculaire voorvallen bij patiënten te verlagen. Verder onderzoek is daarom nodig om het potentieel van dit geneesmiddel te bepalen om het risico op atherosclerotische aandoeningen te verlagen.
De fase 2b, dubbelblinde, gerandomiseerde, placebogecontroleerde MUIR-studie, die gelijktijdig werd gepubliceerd in NEJM, gebruikte een ander siRNA-medicijn, plozasiran, voor de behandeling van gemengde hyperlipidemie [2]. Plozasiran is ontworpen om de expressie van APOC3, het gen dat codeert voor apolipoproteïne C3 (APOC3), een regulator van het TG-metabolisme, in de lever te verminderen, waardoor de TG- en restcholesterolspiegels worden verlaagd. De verlagingen van de TG- en restcholesterolspiegels die in de studie werden waargenomen, waren vergelijkbaar met die in de ARCHES-2-studie. Daarom wordt gespeculeerd dat de twee geneesmiddelen bij patiënten met gemengde hyperlipidemie vergelijkbare effecten hebben op het verlagen van de triglyceridenrijke lipoproteïne en het restcholesterol.
De resultaten van de twee siRNA-onderzoeken laten zien dat dit een veelbelovende klasse medicijnen is die nieuwe mogelijkheden biedt voor de behandeling van gemengde hyperlipidemie en de cardiovasculaire uitkomsten bij patiënten verbetert.
Plaatsingstijd: 15-09-2024